MISSIONE
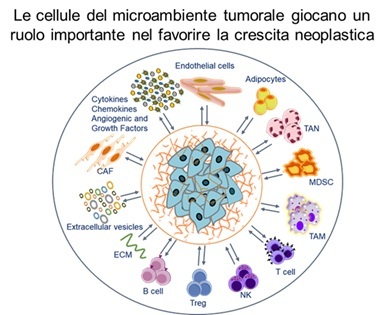
I tumori solidi sono da considerarsi ecosistemi in cui le diverse popolazioni cellulari ed i fattori solubili che compongono il microambiente tumorale (TME) stabiliscono relazioni complesse con le cellule neoplastiche governandone la crescita e tutte quelle funzioni che evolvono nell’acquisizione di un fenotipo invasivo/metastatico.
Il Laboratorio di Modelli Preclinici di Progressione Tumorale svolge attività di ricerca dedicate alla comprensione dei meccanismi molecolari che regolano l’interazione tra cellule tumorali ed il microambiente tumorale (TME).La Mission consiste nell’ identIficare I processi che guidano le diverse fasi della progressione tumorale attraverso lo studio del cross-talk che si realizza tra le cellule neoplastiche, la matrice extracellulare, cellule immunitarie, cellule endoteliali e vescicole extracellulari, chemochine e citochine.
MISSION
Solid tumors should be regarded as complex ecosystems in which the different cellular populations and soluble factors that constitute the tumor microenvironment (TME) establish intricate relationships with neoplastic cells, governing their growth and all those functions that ultimately drive the acquisition of an invasive and metastatic phenotype. The Laboratory of Preclinical Models of Tumor Progression conducts research activities aimed at understanding the molecular mechanisms that regulate the interaction between tumor cells and the tumor microenvironment (TME). Its mission is to identify the processes that orchestrate the various stages of tumor progression by studying the cross-talk occurring among neoplastic cells, the extracellular matrix, immune cells, endothelial cells, extracellular vesicles, chemokines, and cytokines.
RICERCA
I progetti più recenti hanno l’obiettivo di identificare nuovi target di significato prognostico nei tumori solidi ed ematologici, utili per lo sviluppo di nuove strategie terapeutiche con i seguenti end-point: i) identificare i checkpoint immunitari coinvolti nel blocco dell’immunità antitumorale; ii) definire il contributo delle cellule mieloidi, delle vescicole extracellulari e dei fattori solubili (chemochine, citochine, fattori di crescita e proangiogenici) nel sostenere la progressione tumorale; iii) rieducare un TME disfunzionale con farmaci tradizionali e/o di nuova generazione in grado di agire sui checkpoint immunitari coinvolti nel blocco dell’immunità antitumorale e neoangiogenesi.
Le principali linee di ricerca includono:
1) Test preclinici di peptidi ed inibitori capaci di:
• Inibire l’invasione e la metastatizzazione delle cellule tumorali
• Bloccare la neo-angiogenesi ed il mimetismo vascolare
• Modulare l’attività immunosoppressiva delle cellule immunitarie presenti nel TME;
2) Caratterizzare il contributo delle vescicole extracellulari in termini di: composizione, funzioni e potenziale diagnostico, prognostico e predittivo di risposta/resistenza alle terapie standard
3) Validazione preclinica di nuovi approcci teranostici e biomarcatori attraverso modelli preclinici avanzati: il laboratorio sviluppa, ottimizza e valuta nuove molecole da sperimentare come agenti ad attività teranostica.
Un aspetto qualificante è l’attività di traslazione dei risultati preclinici in studi clinici no profit.
Di seguito, alcuni dei progetti di ricerca attualmente in corso:
RESEARCH
Our recent projects aim to identify new targets of prognostic significance in solid tumors, useful for development of new therapeutic strategies with the following end-points: i) dentify the immune checkpoints involved in blocking the antitumor immunity; ii) define the contribution of myeloid cells and soluble factors (chemokines, cytokines, growth and proangiogenic factors) in supporting tumor progression; iii) re-educate a dysfunctional TME with traditional and/or new generation drugs able to act on the immune checkpoints involved in blocking antitumor immunity and neoangiogenesis.
The main research lines include:
1) Preclinical testing of peptides/inhibitors capable of:
• Inhibiting tumor cell invasion and metastasis
• Blocking neo-angiogenesis and vascular mimicry
• Modulating the immunosuppressive activity of immune cells within the TME
2) Characterizing the contribution of extracellular vesicles in terms of: composition, functions, and diagnostic, prognostic, and predictive potential for response or resistance to standard therapies
3) Preclinical validation of new theranostic approaches and biomarkers through advanced preclinical models: the laboratory develops, optimizes, and evaluates new molecules to be tested as agents with theranostic activity
A distinctive feature of the laboratory is its commitment to translating preclinical findings into non-profit clinical studies.
Below are some of the research projects currently underway
Progetto RC 2025-2027 e Studio Clinico Osservazionale – RITMES finanziato dal Ministero della Salute: Ri-educare il Microambiente Tumorale disfunzionale per un approccio terapeutico innovativo del sarcoma. Responsabile scientifico: Dr. Michele Minopoli. Obiettivo del Progetto è ampliare la conoscenza del microambiente tumorale (TME) dei sarcomi utilizzando organoidi multicellulari derivati dal paziente che ci consentiranno di definire il contributo di ogni componente del TME nel sostenere la progressione del sarcoma. Le informazioni ottenute ci consentiranno di raggiungere i seguenti obiettivi: 1) identificare il ruolo dei componenti del TME nel bloccare l’immunità antitumorale e nel supportare l’evasione immunitaria delle cellule del sarcoma; 2) identificare marcatori di significato diagnostico/prognostico; 3) tentare di rieducare un TME disfunzionale con inibitori del checkpoint immunitario e/o farmaci di nuova generazione che contrastano i fattori immunosoppressori e la vasculogenesi
RC Project 2025–2027 and Observational Clinical Study – RITMES funded by the Ministry of Health: Re-educating the dysfunctional Tumor Microenvironment for an innovative therapeutic approach to sarcoma. Principal Investigator: Dr. Michele Minopoli.
The aim of the project exploring tumor microenvironment (TME) role in sarcomas by using patient‑derived multicellular organoids, which will allow us to define the contribution of each TME component in sustaining sarcoma progression. The information obtained will enable us to achieve the following objectives: 1) Identify the role of TME components in blocking antitumor immunity and supporting immune evasion by sarcoma cells;
2) Identify markers of diagnostic/prognostic significance;
3) Attempt to re-educate a dysfunctional TME using immune checkpoint inhibitors and/or new-generation drugs that counteract immunosuppressive factors and vasculogenesis.
Progetto PNRR POC-2022-12376579 – TRUST e Studio Clinico Osservazionale finanziato dal Ministero della Salute: Engineered lisyl oxidase lipid-based nanovesicles for the treatment of solid tumors: on the path to clinical application. Responsabile scientifico dell’UO4: Dr.ssa Maria Vincenza Carriero. L’IRST di Meldola (Emilia Romagna) ha sviluppato vescicole lipidiche (Lipo) funzionalizzate con anticorpi diretti contro l’enzima Lysyl oxidase (LOX) che, overespresso nella matrice del microambiente tumorale (TME) incrementa la capacità invasiva delle cellule neoplastiche e la neovascolarizzazione del tumore. Quando le vescicole lipidiche sono caricate con un chemioterapico, il complesso LipoLox associa l’attività terapeutica dell’anticorpo anti-LOX con la possibilità di concentrare selettivamente il chemioterapico (epirubicina) nel TME. L’obiettivo principale del progetto è comparare la capacità dell’epirubicina libera alla capacità del complesso LIPO-LOX caricato con epirubicina di inibire l’angiogenesi in vitro e ridurre in vivo, in modelli murini, la vascolarizzazione, la crescita e l’invasione di cellule tumorali di sarcoma e carcinoma mammario.
PNRR Project POC‑2022‑12376579 – TRUST and Observational Clinical Study funded by the Ministry of Health: Engineered lysyl oxidase lipid‑based nanovesicles for the treatment of solid tumors: on the path to clinical application. Scientific Coordinator of Unit UO4: Dr. Maria Vincenza Carriero. The IRST in Meldola (Emilia Romagna) has developed lipid vesicles (Lipo) functionalized with antibodies directed against the enzyme Lysyl Oxidase (LOX), and loaded with a chemotherapeutic agent. To date, the LOX overexpression in the extracellular matrix of solid tumors microenvironment (TME), triggers both the invasive capacity of neoplastic cells and endothelial cells neovascularization. The LipoLOX combines the therapeutic activity of the anti LOX antibody with the ability to selectively concentrate the chemotherapeutic drug (epirubicin) within the TME. The main objective of the project is to compare the ability of free epirubicin with that of the LOX targeted LIPO vesicles loaded with epirubicin to inhibit angiogenesis and to reduce vascularization, growth, and invasion of sarcoma and breast carcinoma tumor cells in vitro and in vivo.
Progetto PNRR POC-2023-12377318 – RITAST e Studio Clinico Osservazionale finanziato dal Ministero della Salute: Inibitori radiomarcati di FPR1 per un’applicazione teranostica su tumori solidi. Responsabile scientifico: Dr.ssa Maria Vincenza Carriero. L’obiettivo del progetto è utilizzare un peptide che abbiamo dimostrato inibire eventi chiave che si verificano durante il processo metastatico (motilità cellulare, invasione della matrice extracellulare, formazione di una rete vascolare ed ingresso di cellule tumorali nel flusso sanguigno, prevenendo la formazione di metastasi) come modello per lo sviluppo di analoghi radiomarcati ad attività teranostica, che, attraverso il targeting di FPR1, possano essere utilizzati per la visualizzazione delle lesioni neoplastiche mediante PET ed al contempo esercitare attività citotossica contro le cellule tumorali.
PNRR Project POC‑2023‑12377318 – RITAST and Observational Clinical Study funded by the Ministry of Health: Radiolabeled FPR1 inhibitors for a theranostic application in solid tumors. Principal Investigator: Dr. Maria Vincenza Carriero. The project focuses on inhibitor peptide that, targeting the FPR1 receptor, is able to block several critical steps of the metastatic cascade including tumor cell motility, invasion of the extracellular matrix, formation of new vascular networks, and the entry of cancer cells into the bloodstream. Taking advantage of this molecule as a template, the project aims to develop radiolabeled analogues with theranostic properties. These compounds are designed to serve a dual purpose: enabling precise visualization of tumor lesions through PET imaging, while simultaneously delivering a direct cytotoxic effect to cancer cells. This integrated approach has the potential to enhance both the accuracy of tumor detection and the effectiveness of targeted cancer therapy.
Progetto RC 2025-2027 finanziato dal Ministero della Salute LINEA 3/33_25 Vescicole extracellulari: attori chiave fuori dai sentieri battuti nel superare la resistenza al platino nel carcinoma ovarico e Studio Clinico Osservazionale EPOCA 2025-2027 finanziato dal Ministero della Salute: Individuazione di nuovi marcatori prognostici/predittivi di resistenza al platino nel carcinoma dell’ovaio. Dr.ssa Chiara Ciardiello. La resistenza ai composti del platino rappresenta una sfida cruciale nel carcinoma ovarico avanzato, dove questi farmaci costituiscono lo standard terapeutico iniziale. Nonostante i progressi delle terapie mirate, molte pazienti sviluppano resistenza, rendendo urgente l’identificazione di nuovi biomarcatori predittivi e bersagli terapeutici. Le vescicole extracellulari (EVs), coinvolte nella progressione tumorale e nella farmacoresistenza, trasportano proteine e acidi nucleici tra cellule neoplastiche. In particolare, le Large EVs, inclusi i large oncosomes, risultano arricchite in proteine associate a pathway di resistenza come HSP90, AKT e mTOR. Il progetto prevede la caratterizzazione delle EVs da modelli cellulari resistenti e da plasma di pazienti, integrando i dati con lo studio clinico EPOCA. Saranno valutate la capacità delle EVs di trasferire resistenza, il ruolo di HSP90 e i pathways correlati. Ulteriori attività riguardano lo studio della Vasculogenic Mimicry indotta dalle EVs e la correlazione tra livelli di HSP90 ed esiti clinici. L’obiettivo finale è identificare biomarcatori e strategie terapeutiche innovative per superare la resistenza al platino.
RC Project 2025-2027 funded by the Ministry of Health LINEA 3/33_25 Extracellular Vesicles: Key Off-the-Beaten-Track Players in Overcoming Platinum Resistance in Ovarian Cancer and the EPOCA 2025-2027 Observational Clinical Study funded by the Ministry of Health: Identification of New Prognostic/Predictive Markers of Platinum Resistance in Ovarian Cancer. Dr. Chiara Ciardiello. Resistance to platinum represents a crucial challenge in advanced ovarian cancer, where these drugs are the initial standard of care. Despite advances in targeted therapies, many patients develop resistance, necessitating the identification of new predictive biomarkers and therapeutic targets. Extracellular vesicles (EVs), implicated in tumor progression and drug resistance, transport proteins and nucleic acids between tumor cells. In particular, large EVs, including large oncosomes, are enriched in proteins associated with resistance pathways such as HSP90, AKT, and mTOR. The project involves characterizing EVs from resistant cell models and patient plasma, integrating the data with the EPOCA clinical study. The ability of EVs to transfer resistance, the role of HSP90, and related pathways will be assessed. Additional activities include the study of EV-induced vasculogenic mimicry and the correlation between HSP90 levels and clinical outcomes. The ultimate goal is to identify biomarkers and innovative therapeutic strategies to overcome platinum resistance.
Progetto PNRR-TR1-2023-12377450 finanziato dal Ministero della Salute: Decoding the Extracellular vesicles driven communication in the microenvironment of Hairy cell Leukemia to improve patient care management. Responsabile Scientifico under 40 della UO2: Dr.ssa Chiara Ciardiello. Il progetto esplora il ruolo delle vescicole extracellulari (EV) nella biologia delle “cellule capellute”, tipiche della Hairy cell Leukemia, e nel loro dialogo con il microambiente. L’obiettivo iniziale è identificare una signature biomolecolare delle EV, analizzando il contenuto delle vescicole grandi e piccole circolanti e di quelle prodotte in vitro dalle cellule capellute, per correlare tali profili all’outcome clinico. Il secondo obiettivo approfondisce come le EV derivate dal sangue periferico e, quando disponibile, dal midollo osseo possano modulare l’interazione tra cellule capellute e sistema immunitario, contribuendo a meccanismi di evasione immune. Il terzo obiettivo indaga invece il potenziale delle EV nel regolare il cross-talk tra cellule capellute e cellule stromali, valutando se possano favorire un rimodellamento del microambiente in senso profibrotico. Nel complesso, il progetto mira a chiarire funzioni chiave delle EV nella progressione della malattia, con ricadute potenzialmente rilevanti per la prognosi e per l’identificazione di nuovi bersagli terapeutici.
Project PNRR-TR1-2023-12377450 funded by the Ministry of Health: Decoding the extracellular vesicle-driven communication in the microenvironment of hairy cell leukemia to improve patient care management. Scientific Director (under 40) of UO2: Dr. Chiara Ciardiello. The project explores the role of extracellular vesicles (EVs) in the biology of hairy cells, a hallmark of Hairy Cell Leukemia, and in their interaction with the microenvironment. The initial objective is to identify a biomolecular signature of EVs by analyzing the content of large and small circulating vesicles and those produced in vitro by hairy cells, to correlate these profiles with clinical outcome. The second objective explores how EVs derived from peripheral blood and, when available, bone marrow can modulate the interaction between hairy cells and the immune system, contributing to immune evasion mechanisms. The third objective investigates the potential of EVs to regulate cross-talk between hairy cells and stromal cells, assessing whether they can promote pro-fibrotic remodeling of the microenvironment. Overall, the project aims to clarify key functions of EVs in disease progression, with potentially relevant implications for prognosis and the identification of new therapeutic targets.
Progetto Ricerca Corrente 2025-2027 e Studio Clinico Osservazionale finanziati dal Ministero della Salute Correlazione tra densità mammografica, densità di collagene, infiltrato immunitario e profilo trascrittomico: studio multidimensionale per la valutazione del rischio, la ricerca di nuovi marcatori prognostici e potenziali bersagli terapeutici nel cancro al seno – MADECO. Responsabile scientifico: Dr. Vincenzo Ingangi. Lo scopo principale di questa ricerca è quello di valutare se esiste una correlazione tra il parametro densitometrico della mammografia e la prognosi delle pazienti affette da carcinoma mammario. In particolare verranno studiate specifiche caratteristiche dei tumori mammari (ad esempio densità di fibre di collagene, abbondanza e localizzazione di particolari popolazioni del sistema immunitario all’interno del tessuto tumorale e l’espressione di molecole specifiche). Il nostro obbiettivo è quello di identificare dei fattori dal significato prognostico e dei nuovi potenziali bersagli molecolari per il trattamento del carcinoma mammario.
RC Project 2025-2027 and Observational Clinical Study funded by the Ministry of Health: Correlation between mammographic density, collagen density, immune infiltrate, and transcriptomic profile: a multidimensional study for risk assessment, the search for new prognostic markers, and potential therapeutic targets in breast cancer – MADECO. Principal Investigator: Dr. Vincenzo Ingangi. The primary aim of this research is to evaluate whether there is a correlation between mammography densitometric parameters and the prognosis of breast cancer patients. Specifically, specific characteristics of breast tumors will be studied (e.g., collagen fiber density, abundance and localization of specific immune system populations within tumor tissue, and the expression of specific molecules). Our goal is to identify prognostic factors and potential new molecular targets for breast cancer treatment.
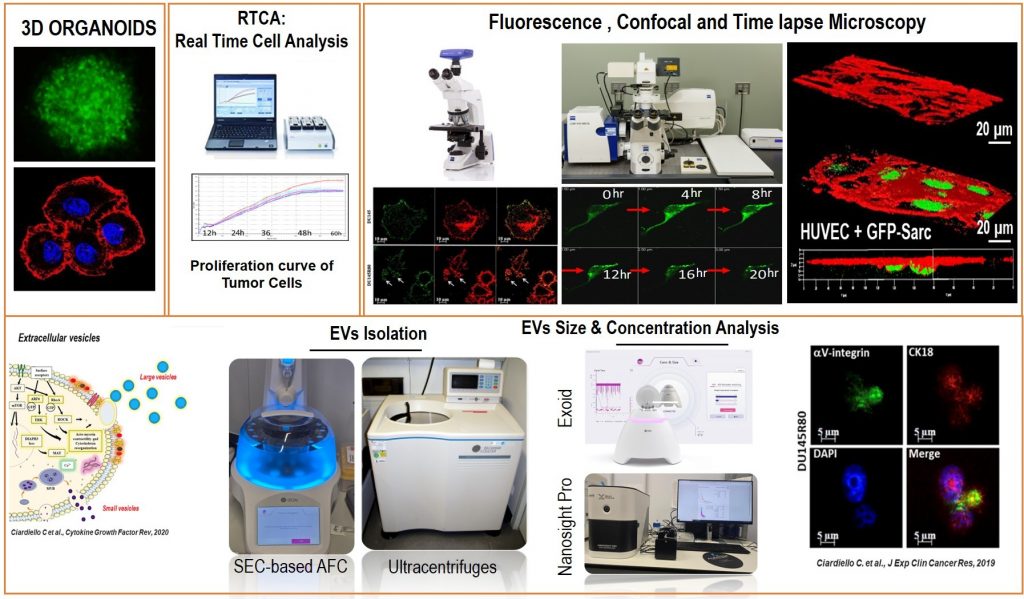
TECNOLOGIE DISPONIBILI ———- AVAILABLE TECHNOLOGIES
PERSONALE ———- PERSONNEL
Direttore/Lab Director Dr. Maria Vincenza Carriero (Biologa/Biologist) ORCID: org/0000-0002-9768-2997 tel. 081 17770581 email: m.carriero@istitutotumori.na.it Dirigenti Sanitari/Staff investigator Dr. Chiara Ciardiello (Biotecnologa/Biotechnologist) ORCID: 0003-2042-8672 tel. 081 17770623 email: c.ciardiello@istitutotumori.na.it Ricercatori Sanitari/Health Researcher: Dr. Michele Minopoli (Biologo/Biologist) ORCID: 0000-0002-5407-481X tel. 081 17770623 email: m.minopoli@istitutotumori.na.it Dr. Vincenzo Ingangi (Biologo/Biologist) ORCID: 0000-0001-5237-8353 tel. 081 17770643 email: vincenzo.ingangi@istitutotumori.na.it Ricercatori Sanitari a tempo determinato/ Health Researcher: Dr. Maurizio Maddalena (Biologo/Biologist) ORCID: 0000-0002-0430-5608 email:maurizio.maddalena@istitutotumori.na.it Dr. Vincenzo Di Vaia (Biologo/Biologist) ORCID: 0009-0002-5573-0935 email: vincenzo.divaia@istitutotumori.na.it Dr. Dominga Amoroso (Biologa/Biologist) ORCID: 0009-0006-1452-5192 email: dominga.amoroso@istitutotumori.na.it Borsisti/Fellows: Dr. Roberta Gatti (Biologa/Biologist) ORCID: 0003-5406-2805 email: roberta.gatti@istitutotumori.na.it Dr. Sara Scala (Biologa/Biologist) ORCID: 0009-0004-1999-2107 email: sara.scala@istitutotumori.na.it Dr. Ametrano Mariateresa (Biotecnologa/Biotechnologist) ORCID: 0009-0002-3448-0375 email:mariateresa.ametrano@istitutotumori.na.it Coll. Profess. Supporto alla ricerca/ Collaborating Researcher: Dr. Gioconda Di Carluccio tel. 081 17770579 ORCID: 0000-0002-3571-9889 email: g.dicarluccio@istitutotumori.na.it Personale in formazione/Staff in training: Dott.ssa Giovanna Caramiello Università di Napoli "Federico II" - Corso di Laurea Magistrale in Biologia Molecolare e Cellulare
PRINCIPALI PUBBLICAZIONI ———- MAIN PUBLICATION
- Ingangi V, Gatti R, Di Carluccio G, Di Vaia V, Cerrone M, Ferrara G, Scala S, Maddalena M, Gallo M, Fazioli F, Ciardiello C, Minopoli M, and Carriero MV. Vasculogenic Mimicry: A Potential Therapeutic Target for Chondrosarcoma Therapy. Cells. 2026; 15(5):392. doi: https://doi.org/10.3390/cells15050392.
- Ingangi V, Amoroso D, Passaro E, Di Vaia V, Maltoni F, Narimanfar G, Minopoli M, Rosa R, Ametrano M, Di Gennaro E, Broccoli A, Zinzani PL, Catani L and Ciardiello C (2026) Understanding hairy cell leukemia in the context of mature B−cell neoplasms: tumor microenvironment and extracellular vesicle contribution to disease pathogenesis. Front. Immunol. 17:1741794. doi: https://doi.org/10.3389/fimmu.2026.1741794.
- Ingangi V, De Chiara A, Ferrara G, Gallo M, Catapano A, Fazioli F, Di Carluccio G, Peranzoni E, Marigo I, Carriero MV, Minopoli M. Emerging Treatments Targeting the Tumor Microenvironment for Advanced Chondrosarcoma. Cells. 2024 Jun 4;13(11):977. doi: https://doi.org/10.3390/cells13110977.
- Castaldo V, Minopoli M, Di Modugno F, Sacconi A, Liguoro D, Frigerio R, Ortolano A, Di Martile M, Gesualdi L, Madonna G, Capone M, Cirombella R, Catizone A, Del Bufalo D, Vecchione A, Carriero MV, Ascierto PA, Mancini R, Fattore L, Ciliberto G. Upregulated expression of miR-4443 and miR-4488 in drug resistant melanomas promotes migratory and invasive phenotypes through downregulation of intermediate filament nestin. J Exp Clin Cancer Res. 2023 Nov 27;42(1):317. doi: https://doi.org/10.1186/s13046-023-02878-9.
- Racanelli D, Brenca M, Baldazzi D, Goeman F, Casini B, De Angelis B, Guercio M, Milano GM, Tamborini E, Busico A, Dagrada G, Garofalo C, Caruso C, Brunello A, Pignochino Y, Berrino E, Grignani G, Scotlandi K, Parra A, Hattinger CM, Ibrahim Mercatali L, De Vita A, Carriero MV, Pallocca M, Loria R, Covello R, Sbaraglia M, Dei Tos AP, Falcioni R, Maestro R. Next-Generation Sequencing Approaches for the Identification of Pathognomonic Fusion Transcripts in Sarcomas: The Experience of the Italian ACC Sarcoma Working Group. Front Oncol. 2020 Apr 15;10:489. doi: https://doi.org/10.3389/fonc.2020.00489
Pubblicazioni del gruppo su Pubmed
CLINICAL TRIALS
- IRSTB142_TRUST – NANOVESCICOLE A BASE DI LIPIDI INGEGNERIZZATE CON LISIL-OSSIDASI PER IL TRATTAMENTO DEI TUMORI SOLIDI: SULLA STRADA DELL’APPLICAZIONE CLINICA. Prot. CEI 22/23 OSS (Delibera N.818 del 19/06/2023).
- RITAST – INIBITORI DI FPR1 RADIOMARCATI PER UN’APPLICAZIONE TERANOSTICA SU TUMORI SOLIDI. Prot. CEI 36/24 OSS (Delibera N.1091 del 17/08/2024).
- EPOCA – INDIVIDUAZIONE DI NUOVI MARCATORI PROGNOSTICI/PREDITTIVI DI RESISTENZA AL PLATINO NEL CARCINOMA DELL’ OVAIO. Prot. CEI 39/22 OSS (Delibera N.1177 del 02/12/2022).
- RITMES – RI-EDUCARE IL MICROAMBIENTE TUMORALE (TME) DISFUNZIONALE PER UN APPROCCIO TERAPEUTICO INNOVATIVO DEL SARCOMA. Prot. CEI 54/22 OSS (Delibera N.60 del 16/01/2023).
- MADECO – CORRELAZIONE TRA DENSITÀ MAMMOGRAFICA, DENSITÀ DI COLLAGENE, INFILTRATO IMMUNITARIO E PROFILO TRASCRITTOMICO: STUDIO MULTIDIMENSIONALE PER LA VALUTAZIONE DEL RISCHIO, LA RICERCA DI NUOVI MARCATORI PROGNOSTICI E POTENZIALI BERSAGLI TERAPEUTICI NEL CANCRO AL SENO. Prot CEI 80/25 OSS (Delibera N.343 del 27/02/2026).
BREVETTI ———- PATENTS
- 2020. Patent N. P3442989: Retro-inverso peptide inhibitors of cell migration, extracellular matrix and endothelial invasion by tumor cells. AUTORI: Carriero MV, Bifulco K, Ciliberto G, Pessi A.
- 2020. Patent N. US20190135863: Retro-inverso peptide inhibitors of cell migration, extracellular matrix and endothelial invasion by tumor cells. AUTORI: Carriero MV, Bifulco K, Ciliberto G, Pessi A.
- 2013. Patent N. US8354374: Peptides having pharmacological activity for treating disorders associated with cell migration, such as cancer. AUTORI: Carriero MV, Pavone V, De Rosa M.