
- MISSIONE/MISSION
La SC “Bersagli Molecolari del Microambiente” svolge attività di ricerca traslazionale prevalentemente orientata allo studio delle interazioni tra le cellule neoplastiche ed il microambiente tumorale (TME – cellule immunitarie, stromali, endoteliali, cito-chemiochine, fattori solubili) nei tumori solidi primitivi e secondari. La mission della struttura è la caratterizzazione delle interazioni tra tumore/microambiente tumorale per identificare meccanismi responsabili della progressione tumorale, di resistenza a terapie e nuovi targets diagnostico/terapeutici.
L’attività della UOC, in linea con le finalità di ricerca traslazionale dell’Istituto, è basata su una intensa attività multidisciplinare derivante dalla collaborazione con Unità Chirurgiche, Mediche e Diagnostiche inoltre la UOC “Bersagli molecolari del microambiente” conduce e partecipa a Progetti di Ricerca nazionali ed internazionali con finalità precliniche e di ricerca traslazionale clinica.
The “Microenvironment Molecular Targets” Unit carries out translational research activities focused on the interactions between neoplastic cells and tumor microenvironment (TME – immune -, stromal-, endothelial cells, cyto-chemokines, soluble factors) in primary and secondary solid tumors. The main objective is to identify mechanisms responsible for tumor progression, resistance to therapies and new diagnostic/therapeutic targets within the TME. Research program focuses, in line with the translational research purposes of the Institute, on intense multidisciplinary activity through collaboration with Surgical, Medical and Diagnostic Units. Furthermore, the “Microenvironment Molecular Targets” Unit conducts and participates in national and international Research Projects with preclinical and clinical translational research purposes.
- RICERCA/RESEARCH
La UOC “Bersagli molecolari del microambiente” svolge attività di ricerca meccanicistica/traslazionale rivolta allo studio delle alterazioni fenotipiche e funzionali delle cellule neoplastiche e delle cellule del microambiente tumorale. Inoltre, la UOC “Bersagli molecolari del microambiente” propone e partecipa ad attività di ricerca Traslazionale Clinica rivolta allo sviluppo di modelli per la valutazione di farmaci con meccanismi di azione e/o bersagli molecolari innovativi.
La ricerca si articola nelle seguenti linee di ricerca:
- Design e sviluppo di nuove molecole in grado di inibire la progressione tumorale attraverso bersagli identificati nel microambiente tumorale.
- Sviluppo di nuovi approcci diagnostico-teranostici.
- Nuovi approcci per la identificazione e caratterizzazione di biomarcatori utili al monitoraggio della malattia e/o predittivi di risposta ai trattamenti nel sangue periferico (cellule tumorali circolanti e specifiche popolazioni immunitarie).
The “Microenvironment Molecular Targets” Unit carries out mechanistic/translational research aimed at studying the phenotypic and functional alterations of neoplastic and TME cells. Moreover, the “Microenvironment Molecular Targets” propose and participate to Clinical Translational research aimed at developing models for the evaluation of drugs with innovative mechanisms of action and/or molecular targets.
The research program relies on:
- Design and development of new therapeutic molecules with target in TME.
- Development of new diagnostic-theranostic approaches.
- Peripheral prognostic and predictive biomarkers (circulating tumor cells and specific immune cell populations).
Design e sviluppo di nuove molecole in grado di inibire la progressione tumorale.
Una nuova classe di antagonisti peptidici del CXCR4 è stata sviluppata e brevettata dal nostro laboratorio. CXCR4 è un recettore per chemochina in grado di favorire la crescita, le metastasi, “escape” immunologico e resistenza a terapia. La modulazione del CXCR4 modifica anche la composizione del microambiente tumorale promuovendo l’ingresso di cellule immuno attive. La modifica del microambiente tumorale può sensibilizzare le neoplasie all’azione dell’immunoterapia mediata da inibitori dei checkpoints immunitari (ICI).
Development of new molecules inhibiting tumor progression
A new class of CXCR4-peptide antagonists has been developed and patented by our laboratory. CXCR4 is a chemokine receptor that promotes growth, metastasis, immune escape, and therapy resistance. CXCR4 targeting modifies the composition of the tumor microenvironment by promoting immune-active cells infiltration. Tumor microenvironment targeting may sensitize tumors to immunotherapy through immune checkpoint inhibitors (ICI).
Sviluppo di nuovi approcci diagnostico-teranostici.
Attualmente la diagnosi e la valutazione della risposta alle terapie si basa su immagini PET-CT. [18F]-FDG risulta il tracciante PET più comunemente utilizzato. Esistono però limitazioni relative al metabolismo di alcune neoplasie e l’utilizzo di bersagli molecolari potrebbe migliorare la caratterizzazione dei tumori, sia di lesioni primarie che secondarie. CXCR4 è iperespresso nella maggior parte dei tumori ematologici e solidi, nelle cellule tumorali e nel microambiente tumorale. L’imaging basato su CXCR4 gioca un ruolo cruciale nella diagnosi precoce di lesioni primarie e secondarie positive al CXCR4 e potrebbe predire l’efficacia di terapie che hanno come bersaglio questo recettore. Abbiamo recentemente sviluppato una sonda PET anti-CXCR4 [68Ga]Ga-R54in grado di riconoscere le lesioni CXCR4+con elevata sensibilità e specificità. Il peptide utilizzato per lo sviluppo della sonda diagnostica può essere coniugato a radionuclidi terapeutici.
Development of new diagnostic-theranostic approaches. Currently, the diagnosis and the assessment response to therapies relies on PET-CT imaging. [18F]F-FDG is the PET tracer most commonly in use . However, tumor metabolism may limit the use of [18F]F-FDG and molecular targeting improves tumor characterization, primary and secondary lesions. CXCR4 is overexpressed in the majority of haematological and solid tumors, in cancer cells and at the TME level. CXCR4 molecular imaging plays a central role for the early detection of CXCR4 primary and secondary lesions and may predict CXCR4 targeted therapies efficacy. A new CXCR4 targeted PET tracer [68Ga]Ga-R54 was recently developed recognizing anti- CXCR4+ lesions with high sensitivity and specificity. The peptide used for the development of the diagnostic probe can be conjugated to therapeutic radionuclides.
Nuovi approcci per la identificazione e caratterizzazione di biomarcatori prognostici e/o predittivi di risposta ai trattamenti nel sangue periferico (cellule tumorali circolanti e specifiche popolazioni immunitarie).
I biomarcatori sono indicatori di processi fisiologici, patologici o di risposta al trattamento terapeutico. I biomarcatori consentono l’identificazione di pazienti che potrebbero trarre beneficio da una determinata terapia o quelli per i quali la tossicità correlata potrebbe essere rilevante, consentendo anche di predire la risposta al trattamento. In particolare, biomarcatori prognostici e predittivi saranno ricercati e validati in tumori primari e/o secondari e nel sangue periferico di pazienti con cancro del rene, ovaio, endometrio e vescica tra gli altri.
New approaches for the identification and characterization of prognostic and predictive in peripheral blood (circulating tumor cells and specific immune populations).
Biomarkers are an objective and quantifiable indicators of a physiological process, pathological processes or responses to treatment. Biomarkers are a clear unmet need. Biomarkers could identify patients that will benefit from a therapy, for whom the toxicity is worth and may predict outcome. In particular prognostic and predictive biomarkers will be searched and validated in primary/secondary tumors, peripheral blood of patients with renal cancer, ovarian, endometrium abd bladder cancer among others.
GRANTS E PROGETTI/GRANTS AND PROJECTS
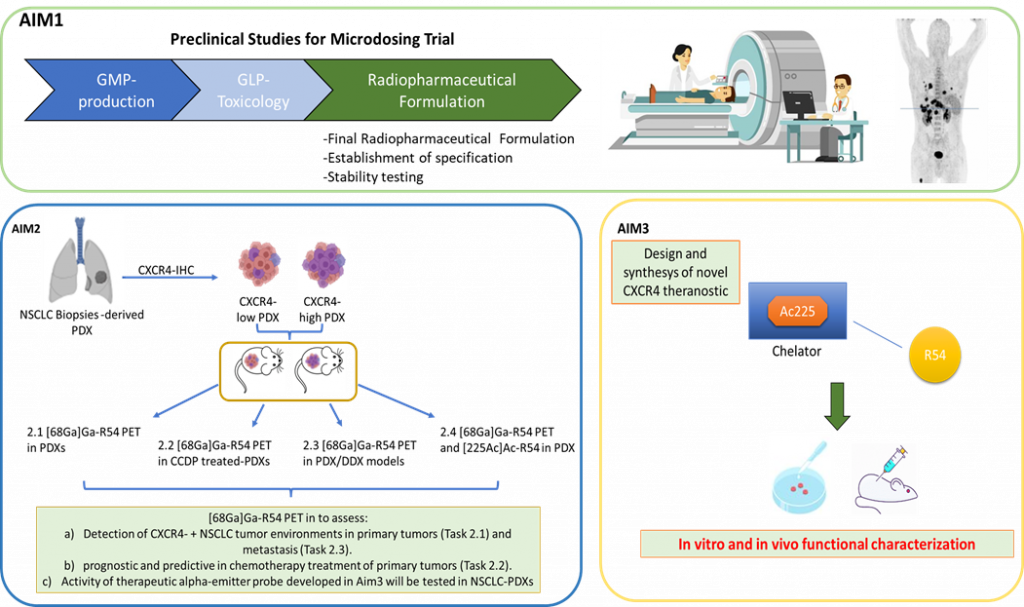
PNRR-POC-2022-12376329– Italian Ministry of Health – 2023-2025 – PI Dr. Stefania Scala (N. 625 del 24/05/2023)“From diagnostic to theranostic CXCR4-targeting PET probe. Proof of concept in Non Small Cell Lung Cancer (NSCLC)-PDX model”. Questo studio prevede il coordinamento tra UO1 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale), UO2 (Fondazione IRCCS Istituto Nazionale dei Tumori di Milano) and UO3 (Università degli Studi della Campania “L. Vanvitelli) con obiettivi: 1. lo sviluppo del PET tracer [68Ga]GaR54 specifico per CXCR4; 2. studio di fase 1 nell’uomo e valutazione dell’efficacia in modelli pre-clinici di cancro al polmone 3. lo sviluppo della controparte terapeutica [225Ac] Ac-R54 che sarà valutata in modelli di topo.
PNRR-POC-2022-12376329 – Italian Ministry of Health – 2023-2025 – PI Dr. Stefania Scala (N. 625 del 24/05/2023)“From diagnostic to theranostic CXCR4-targeting PET probe. Proof of concept in Non Small Cell Lung Cancer (NSCLC)-PDX model”. This study protocol involves the coordination between UO1 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale), UO2 (Fondazione IRCCS Istituto Nazionale dei Tumori di Milano) and UO3 (Università degli Studi della Campania “L. Vanvitelli) to aims: 1. development of the CXCR4-specific [68Ga]GaR54 PET tracer; 2. phase 1 study in humans and evaluation of efficacy in preclinical models of lung cancer; 3. development of the therapeutic counterpart [225Ac] Ac-R54 that will be evaluated in mouse models.
PNRR-TR1-2023-12377199 – Italian Ministry of Health – 2024-2026 – UO Leader: Dr. Stefania Scala (N.1045 del 21/08/2024) “New preclinical and clinical approaches to mesothelioma, an archetypal inflammatory tumor”. Questo studio prevede il coordinamento tra UO1 (IRCCS San Raffaele Hospital) and UO2 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale) per indagare il ruolo di HMGB1 e CXCR4 nel trattamento del mesotelioma e la formazione di metastasi.
PNRR-MCNT2-2023-12377496 – Italian Ministry of Health –2024-2026 – UO Leader: Dr. Caterina Ieranò (N.1029 del 09/08/2024) “Targeting therapy-induced paracrine signaling pathways in prostate cancer to prevent disease progression and resistance” Questo studio prevede il coordinamento tra UO1 (Policlinico Universitario Tor Vergata), UO2 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale) and UO3 (Università degli Studi Dell’Aquila) per indagare il ruoli degli eicosanoidi e del sistema CXCR4/CXCL12 nella ripopolamento indotto dalla terapia e nell’incremento della malignità del cancro alla prostata metastatico.
5XMILLE_2022_20 – 2024-2026 – PI: Dr. Stefania Scala (N.994 del 07/08/2024) “Sviluppo di nanovettori a doppio bersaglio CXCR4 e FAP-1 per la diagnosi precoce e trattamento del carcinoma pancreatico” il cui obiettivo è sviluppare una sonda diagnostica/terapeutica bi-specifica per FAP e CXCR4 da utilizzare nell’adenocarcinoma duttale pancreatico (PDAC).
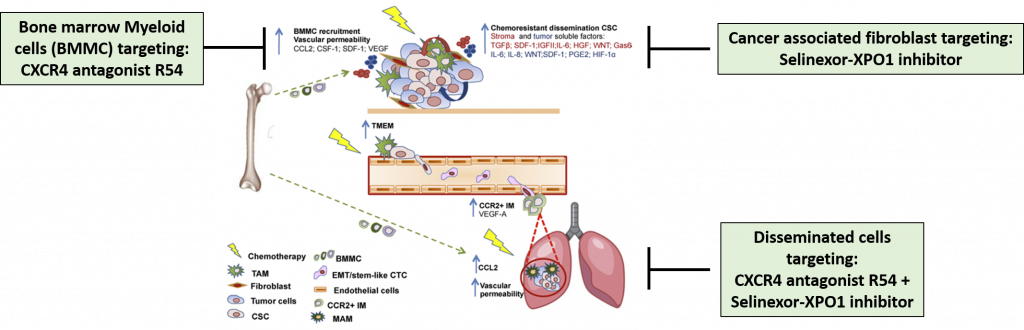
RF-2021-12371959 – Italian Ministry of Health – 2024-2026, UO Leader: Dr. Crescenzo D’Alterio: “Tackling immunomodulatory properties of stromal cells to improve therapeutic strategies in lung cancer“. Questo studio prevede il coordinamento tra Istituto Nazionale Tumori – IRCCS Milan (UO1), Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale (UO2), and Università di Milano – Bicocca (UO3). Obiettivi: Analisi dell’eterogeneità dei fibroblasti di polmone e delle loro funzioni immunosoppressive e identificazione di bersagli attraverso analisi scRNA-seq effettuati su tessuti ottenuti da pazienti affetti da cancro ai polmoni trattati con cisplatino. E’ previsto lo studio dell’asse CXCR4-CXCL12 nel microambiente tumorale attraverso saggi in vitro con cellule tumorali di polmone e fibroblasti associati usando antagonisti di CXCR4 e XPO.(UO2, Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale).
PNRR-TR1-2023-12377199 – Italian Ministry of Health – 2024-2026 – UO Leader: Dr. Stefania Scala (N.1045 del 21/08/2024) “New preclinical and clinical approaches to mesothelioma, an archetypal inflammatory tumor”. This study protocol involves the coordination between UO1 (IRCCS San Raffaele Hospital) and UO2 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale) to explore the role of HMGB1 and CXCR4 in mesothelioma treatment and metastasis.
PNRR-MCNT2-2023-12377496 – Italian Ministry of Health –2024-2026 – UO Leader: Dr. Caterina Ieranò (N.1029 del 09/08/2024) “Targeting therapy-induced paracrine signaling pathways in prostate cancer to prevent disease progression and resistance” This study protocol involves the coordination between UO1 (Policlinico Universitario Tor Vergata), UO2 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale) and UO3 (Università degli Studi Dell’Aquila) to explore the role of eicosanoids and the CXCR4/CXCL12 system in therapy-induced repopulation and increased malignancy of metastatic prostate cancer cells.
5XMILLE_2022_20 – 2024-2026 – PI: Dr. Stefania Scala (N.994 del 07/08/2024) “Sviluppo di nanovettori a doppio bersaglio CXCR4 e FAP-1 per la diagnosi precoce e trattamento del carcinoma pancreatico” to aims the development of a diagnostic/therapeutic probe with dual FAP/CXCR4 targeting in pancreatic ductal adenocarcinoma (PDAC).
RF-2021-12371959 – Italian Ministry of Health – 2024-2026, UO Leader: Dr. Crescenzo D’Alterio: “Tackling immunomodulatory properties of stromal cells to improve therapeutic strategies in lung cancer“. Coordination between Istituto Nazionale Tumori – IRCCS Milan (UO1), National Cancer Institute “Fondazione Pascale” (UO2), and Università di Milano – Bicocca (UO3). Aims: Analyze lung fibroblast heterogeneity and immunosuppressive functions, identifying targets via scRNA-seq from cisplatin-treated lung cancer patient tissues. Explore CXCR4-CXCL12’s role in the tumor microenvironment through in vitro assays with lung cancer cells and fibroblasts using CXCR4 and XPO antagonists at UO2 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale).
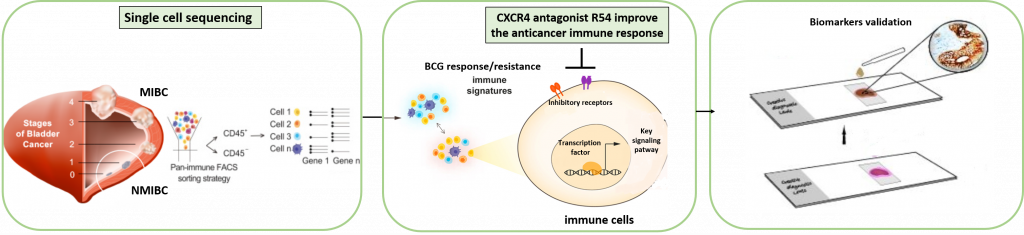
PNRR-MAD-2022-12376756 – Italian Ministry of Health – 2023-2025 (N.787 del 05/07/2023), UO Leader Dr. Crescenzo D’Alterio: “Single cell dissection of the tumor microenvironment in bladder cancer for the identification of predictive tools and new therapies“. Questo studio prevede il coordinamento tra IRCCS Istituto Clinico Humanitas (UO1) e Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale (UO2). Obiettivi: Tracciamento del profilo del microambiente tumorale e identificazione di fattori prognostici e biomarcatori predittivi per la resistenza al BCG. Studio preclinico del fenotipo delle cellule NK derivate da paziente e della loro funzione nel carcinoma della vescica muscolo-infiltrante e non muscolo-infiltrante, valutando il ruolo del Sistema CXCR4-CXCL12 nell’ immunosoppressione (UO2, Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale).
PNRR-MAD-2022-12376756 – Italian Ministry of Health – 2023-2025 (N.787 del 05/07/2023), UO Leader Dr. Crescenzo D’Alterio: “Single cell dissection of the tumor microenvironment in bladder cancer for the identification of predictive tools and new therapies“. Coordination between IRCCS Istituto Clinico Humanitas (UO1) and National Cancer Institute “Fondazione Pascale” (UO2). Aims: Profile the tumor microenvironment and identify prognostic factors and predictive biomarkers for BCG resistance. Preclinical investigation of patient derived NK cell phenotype and function in muscle-invasive and non-muscle-invasive bladder cancer, exploring CXCR4-CXCL12’s role in immunosuppression at UO2 (Istituto Nazionale Tumori di Napoli – IRCCS G. Pascale).
RC 2025-2027 Linea 2/12– Italian Ministry of Health – PI Dr. Stefania Scala – “Biomarcatori prognostici e predittivi di risposta all’immunoterapie nuovi target terapeutici nel microambiente tumorale”. Obiettivi del progetto: 1. Definire il fenotipo delle cellule immunitarie periferiche nei pazienti mRCC allo stadio avanzato, trattati in prima linea con TKI-ICI o ICI-ICI. 2. Identificare nuovi bersagli terapeutici nel microambiente tumorale.
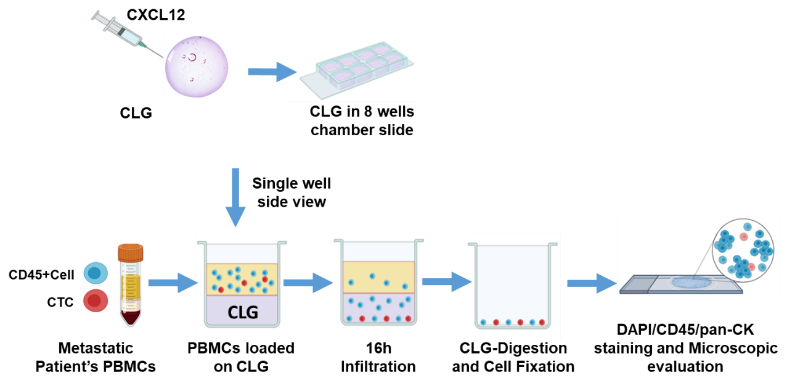
RC 2025-2027 Linea 1/08– Italian Ministry of Health – PI Dr. Luigi Portella – “Hydrogel a base di acido ialuronico caricato con CXCL12 (CLG) come nuovo dispositivo per l’isolamento e la caratterizzazione delle Cellule Tumorali Circolanti con proprietà invasive”. Obiettivi dello studio: 1. Stimare il valore prognostico delle CLG-CTCs nei pazienti con cancro all’ovaio e cancro ai polmoni in stadio avanzato. 2. Caratterizzazione a livello molecolare delle CLG-CTCs isolate tramite TRAP4MET-1 a singola cellula 3. Generazione di modelli 3D derivati da CLG-CTCs (CTCDO).
RC 2025-2027 Linea 2/12– Italian Ministry of Health – PI Dr. Stefania Scala – “Biomarcatori prognostici e predittivi di risposta all’immunoterapiae nuovi target terapeutici nel microambiente tumorale”. The project aims to: Define peripheral immunophenotype in first line treated TKI-ICI or ICI-ICI advanced/mRCC patients. 2. Identify new therapeutic targets in TME
RC 2025-2027 Linea 1/08– Italian Ministry of Health – PI Dr. Luigi Portella – “Hydrogel a base di acido ialuronico caricato con CXCL12 (CLG) come nuovo dispositivo per l’isolamento e la caratterizzazione delle Cellule Tumorali Circolanti con proprietà invasive”. The project aims to: 1. Assess the prognostic value of CLG-CTCs in patients with ovarian cancer and advanced lung cancer. 2. Molecularly characterize CLG-CTCs isolated in TRAP4MET-1 at single cell level. 3. Generate 3D models derived from CLG-CTCs (CTCDO).
RC 2025-2027– Italian Ministry of Health – PI Dr. Anna Maria Trotta – “Studio del microambiente tumorale e periferico in pazienti affette da neoplasie primitive dell’ovaio: focus sulle cellule Natural Killer simil-deciduali.” Obiettivi del progetto: 1. Caratterizzazione delle cellule NK simil-deciduali ottenute da sangue periferico e/o da tessuto tumorale dei pazienti con OC. Ruolo prognostico. 2. Interazione In vitro tra cellule NK ottenute dai pazienti OC (sangur periferico e tessuto tumorale) e cellule di cancro ovarico. 3. Valutazione in vivo degli effetti dell’asse CXCR4-CXCL12 sulle cellule NK.
RC 2025-2027– Italian Ministry of Health – PI Dr. Anna Maria Trotta – “Studio del microambiente tumorale e periferico in pazienti affette da neoplasie primitive dell’ovaio: focus sulle cellule Natural Killer simil-deciduali.” The project aims to: 1. Characterization of decidual-like NK cells from peripheral blood/tumor tissue of patients with OC. Prognostic significance. 2. In vitro interaction of NK cells from OC patients (peripheral and tumoral) and ovarian cancer cells. 3. In vivo evaluation of the effect of the CXCR4-CXCL12 axis on NK cells.
RC 2025-2027– Italian Ministry of Health – PI Dr. Caterina Ieranò – “Meccanismi di resistenza agli inibitori dei checkpoints immunitari nelle neoplasie dell’endometrio: focus p53”. Obiettivi dello studio: 1. Presentazione dell’antigene e morte cellulare indotta dal sistema immunitario come meccanismo di primaria resistenza agli ICI e evasion immunitaria. 2. Associazione tra fenotipo immunitario periferico e TME nei pazienti con carcinama endometriale (p53 mut versus p53 wt). 3. Meccanismi di resistenza all’Avelumab nelle linee cellulari di carcinoma endometriale con differenti mutazioni a carico di TP53.
RC 2025-2027– Italian Ministry of Health – PI Dr. Caterina Ieranò – “Meccanismi di resistenza agli inibitori dei checkpoints immunitari nelle neoplasie dell’endometrio: focus p53”. The project aims to: 1. Antigen presentation machinery and immunogenic cell death as mechanisms of primary resistance to ICIs and immune evasion. 2. Association between peripheral immunophenotype and TME in primary endometrial cancer patients p53 mut versus p53 wt. 3. Mechanisms of resistance to Avelumab in endometrial cancer cell lines with different TP53 mutational status.
AIRC_ID_24746– PI Dr. Stefania Scala (N.1018 del 08/10/2021) “New generetion of CXCR4 antagonist: peptide R54 from biomolecular mechanism to first in man clinical study” – IG 24746. Lo studio ha lo scopo di valutare l’efficacia del peptide R54, antagonista del CXCR4, come molecola antitumorale in grado di inibire la crescita tumorale, lo sviluppo di metastasi e potenziare l’efficacia degli ICI. Inoltre, R54 sarà la base per lo sviluppo di [68Ga]NOTA-Ahx-R54, una sonda PET specifica per CXCR4, da utilizzare come nuovo strumento per la diagnosi precoce di lesioni primarie o secondarie in pazienti con tumori che iperesprimono CXCR4.
AIRC_ID_24746– PI Dr. Stefania Scala (N.1018 del 08/10/2021) “New generetion of CXCR4 antagonist: peptide R54 from biomolecular mechanism to first in man clinical study” – IG 24746 The prject aims to develop the CXCR4 antagonist R54 as anticancer drug inhibiting tumor growth, metastasis development and potentiating efficacy of ICI. Moreover, R54 will be the backbone for the development of [68Ga]NOTA-Ahx-R54, a CXCR4 specific PET tracer as new diagnostic tool for early detection of primary and secondary lesions in patients with CXCR4 overexpressing tumors.
Brevetti/Patents
• “CYCLIC PEPTIDES BINDING CXCR4 RECEPTOR AND RELATIVE MEDICAL AND DIAGNOSTIC USES” EP2528936B9, WO 2011/092575
• “RADIOLABELED PEPTIDES FOR NON-INVASIVE DIAGNOSIS AND TREATMENT OF CXCR4 EXPRESSING TUMORS” WO2021130329
3. STAFF E PERSONALE/STAFF AND PERSONNEL
Direttore/Director
Stefania Scala (MD, PhD) – 08117770596 – s.scala@istitutotumori.na.it (ORCID: 0000-0001-9524-2616
Dirigenti/Staff Scientists
Daniela Califano, Master Degree in Biology -08117770592 d.califano@istitutotumori.na.it ORCID: 0000-0001-6945-3209
Crescenzo D’Alterio, PhD – 08117770594- c.dalterio@istitutotumori.na.it (ORCID: 0000-0003-0275-3367)
Luigi Portella, Master Degree in Biology Biotechnology – 08117770593 – l.portella@istitutotumori.na.it (ORCID: 0000-0002-8679-3309)
Ricercatori Sanitari/Staff Researchers
Francesca Galdiero, Master Degree in Biology – f.galdiero@istitutotumori.na.it (ORCID: 0000-0001-7682-5381)
Caterina Ieranò, PhD ,c.ierano@istitutotumori.na.it (ORCID: 0000-0003-3138-1873)
Daniela Russo, Master Degree in Biology– d.russo@istitutotumori.na.it (ORCID: 0000-0001-9471-1935)
Sara Santagata, PhD – s.santagata@istitutotumori.na.it (ORCID: 0000-0001-8680-084X)
Anna Maria Trotta, Master Degree in Biology – am.trotta@istitutotumori.na.it (ORCID: 0000-0003-4110-2057)
Giuseppina Rea, PhD- g.rea@istitutotumori.na.it (ORCID: 0000-0002-5420
Ricercatori (Tempo determinato)/Researchers (Fixed Term)
Cinzia Vetrei, PhD– cinzia.vetrei@istitutotumori.na.it (ORCID: 0000-0002-1520-540X)
Federica Auletta, PhD – federica.auletta@istitutotumori.na.it (ORCID: 0000-0001-7874-6847)
Giuseppe Guardascione, PhD – giuseppe.guardascione@istitutotumori.na.it (ORCID: 0000-0003-4272-7948)
Pasqualina Pagano, PhD – pasqualina.pagano@istitutotumori.na.it (ORCID: 0009-0008-3609-018X)
Fabrizio Licitra PhD – fabrizio.licitra@istitutotumori.na.it (ORCID: 0000-0001-8528-6623)
Rosa Catapano, Master Degree in Biology,- rosa.catapano@istitutotumori.na.it (ORCID: 0009-0002-5129-6991)
Borsisti/Fellows
Dario Guido di Febbraro, Biologist – darioguido.difebbraro@istitutotumori.na.it (ORCID: 0009-0003-2546-9665)
Gaetana Di Maiolo, Biologist – gaetana.dimaiolo@istitutotumori.na.it (ORCID: 0009-0008-6237-7475)
Tecnici di Laboratorio/Lab Technicians
Tommaso Ambrosio – tommaso.ambrosio@istitutotumori.na.it
4. PRINCIPALI PUBBLICAZIONI (ultimi 5 anni)/MAIN SCIENTIFIC PUBLICATION (last 5 years)
Russo D, Spina A, Portella L, Bello AM, Galdiero F, Trotta AM, Ieranò C, Rea G, Cecere SC, Coppola E, Di Maro S, Pignata S, Califano D, Scala S. The CXCR4 antagonist R54 targets epithelial-mesenchymal transition (EMT) in human ovarian cancer cells.PLoS One. 2024 Dec 19;19(12):e0314735. doi: 10.1371/journal.pone.0314735. eCollection 2024. PMID: 39700131
Trotta AM, Mazzarella V, Roggia M, D’Aniello A, Del Bene A, Vetrei C, Di Maiolo G, Campagna E, Natale B, Rea G, Santagata S, D’Alterio C, Cutolo R, Mottola S, Merlino F, Benedetti R, Altucci L, Messere A, Cosconati S, Tomassi S, Scala S, Di Maro S. Comprehensive structural investigation of a potent and selective CXCR4 antagonist via crosslink modification. Eur J Med Chem. 2024 De5;279:116911. doi: 10.1016/j.ejmech.2024.116911. Epub 2024 Sep 25. PMID: 39348763
Portella L, Bertolini G, Guardascione G, Di Febbraro DG, Ieranò C, D’Alterio C, Rea G, Napolitano M, Santagata S, Trotta AM, Camerlingo R, Scarpa E, Cecere SC, Ottaiano A, Palumbo G, Morabito A, Somma T, De Rosa G, Mayol L, Pacelli R, Pignata S, Scala S. CXCL12-loaded-hydrogel (CLG): A new device for metastatic circulating tumor cells (CTCs) capturing and characterization.Heliyon. 2024 Jul 31;10(15):e35524. doi: 10.1016/j.heliyon.2024.e35524. eCollection 2024 Aug 15. PMID: 39170328
Santagata S, Trotta AM, D’Alterio C, Napolitano M, Rea G, Di Napoli M, Portella L, Ieranò C, Guardascione G, Coppola E, Caux C, Dubois B, Boyle HJ, Carles J, Rossetti S, Azzaro R, Feroce F, Perdonà S, Fordellone M, Bello AM, Califano D, Chiodini P, Pignata S, Scala S. KIR2DL2/DL3+NKs and Helios+Tregs in Peripheral Blood Predict Nivolumab Response in Patients with Metastatic Renal Cell Cancer.Clin Cancer Res. 2024 Oct 15;30(20):4755-4767. doi: 10.1158/1078-0432.CCR-24-0729. PMID: 39167621
Trotta AM, Tomassi S, Di Maiolo G, Ieranò C, Vetrei C, D’Alterio C, Merlino F, Messere A, D’Aniello A, Del Bene A, Mazzarella V, Roggia M, Natale B, Cutolo R, Campagna E, Mottola S, Russo R, Chambery A, Benedetti R, Altucci L, Cosconati S, Scala S, Di Maro S. Disulfide bond replacement with non-reducible side chain to tail macrolactamization for the development of potent and selective CXCR4 peptide antagonists endowed with flanking binding sites.Eur J Med Chem. 2024 Oct 5;276:116669. doi: 10.1016/j.ejmech.2024.116669. Epub 2024 Jul 14. PMID: 39053189
Santagata S, Rea G, Bello AM, Capiluongo A, Napolitano M, Desicato S, Fragale A, D’Alterio C, Trotta AM, Ieranò C, Portella L, Persico F, Di Napoli M, Di Maro S, Feroce F, Azzaro R, Gabriele L, Longo N, Pignata S, Perdonà S, Scala S. Targeting CXCR4 impaired T regulatory function through PTEN in renal cancer patients Br J Cancer. 2024 Jun;130(12):2016-2026. doi: 10.1038/s41416-024-02702-x. Epub 2024 May 4. PMID: 38704478
Santagata, S., Rea, G., Castaldo, D., Napolitano, M., Capiluongo, A., D’Alterio, C., Trotta, A.M., Ieranò, C., Portella, L., Di Maro, S., Tatangelo, F., Albino, V., Guarino, R., Cutolo, C., Izzo, F., Scala, S. Hepatocellular carcinoma (HCC) tumor microenvironment is more suppressive than colorectal cancer liver metastasis (CRLM) tumor microenvironment (2023) Hepatology International
D’Alterio C., Giardino A., Scognamiglio G., Butturini G., Portella L., Guardascione G., Frigerio I., Montella M., Gobbo S., Martignoni G., Napolitano V., De Vita F., Tatangelo F., Franco R., Scala S. CXCR4-CXCL12-CXCR7 and PD-1/PD-L1 in Pancreatic Cancer: CXCL12 Predicts Survival of Radically Resected Patients (2022) Cells, 11 (21), art. no. 3340, DOI: 10.3390/cells11213340
D’Alterio, C.; Spina, A.; Arenare, L.; Chiodini, P.; Napolitano, M.; Galdiero, F.; Portella, L.; Simeon, V.; Signoriello, S.; Raspagliesi, F.; Lorusso, D.; Pisano, C.; Colombo, N.; Zannoni, G.F.; Losito, N.S.; De Cecio, R.; Scognamiglio, G.; Califano, D.; Russo, D.; Tuninetti, V.; Piccirillo, M.C.; Gargiulo, P.; Perrone, F.; Pignata, S.; Scala, S. Biological Role of Tumor/Stromal CXCR4-CXCL12-CXCR7 in MITO16A/MaNGO-OV2 Advanced Ovarian Cancer Patients. Cancers (2022), 14, 1849. https://doi.org/10.3390/cancers14071849
Ieranò C, Righelli D, D’Alterio C, Napolitano M, Portella L, Rea G, Auletta F, Santagata S, Trotta AM, Guardascione G, Liotti F, Prevete N, Maiolino P, Luciano A, Barbieri A, Di Mauro A, Roma C, Esposito Abate R, Tatangelo F, Pacelli R, Normanno N, Melillo RM and Scala S. In PD-1+ human colon cancer cells NIVOLUMAB promotes survival and could protect tumor cells from conventional therapies. (2022) Journal for ImmunoTherapy of Cancer
Santagata, S., Ieranò, C., Trotta, A.M., Capiluongo, A., Auletta, F., Guardascione, G., Scala, S. CXCR4 and CXCR7 Signaling Pathways: A Focus on the Cross-Talk Between Cancer Cells and Tumor Microenvironment (2021) Frontiers in Oncology, 11, art. no. 591386, . DOI: 10.3389/fonc.2021.591386
Trotta, A.M., Aurilio, M., D’Alterio, C., Ieranò, C., Di Martino, D., Barbieri, A., Luciano, A., Gaballo, P., Santagata, S., Portella, L., Tomassi, S., Marinelli, L., Sementa, D., Novellino, E., Lastoria, S., Scala, S., Schottelius, M., Di Maro, S. Novel Peptide-Based PET Probe for Non-invasive Imaging of C-X-C Chemokine Receptor Type 4 (CXCR4) in Tumors (2021) Journal of Medicinal Chemistry, 64 (6), pp. 3449-3461. DOI: 10.1021/acs.jmedchem.1c00066
D’Alterio, C., Zannetti, A., Trotta, A.M., Ieranò, C., Napolitano, M., Rea, G., Greco, A., Maiolino, P., Albanese, S., Scognamiglio, G., Tatangelo, F., Tafuto, S., Portella, L., Santagata, S., Nasti, G., Ottaiano, A., Pacelli, R., Delrio, P., Botti, G., Scala, S. New CXCR4 antagonist peptide R (Pep R) improves standard therapy in colorectal cancer (2020) Cancers, 12 (7), art. no. 1952, pp. 1-16. DOI: 10.3390/cancers12071952
D’Alterio, C., Buoncervello, M., Ieranò, C., Napolitano, M., Portella, L., Rea, G., Barbieri, A., Luciano, A., Scognamiglio, G., Tatangelo, F., Anniciello, A.M., Monaco, M., Cavalcanti, E., Maiolino, P., Romagnoli, G., Arra, C., Botti, G., Gabriele, L., Scala, S. Targeting CXCR4 potentiates anti-PD-1 efficacy modifying the tumor microenvironment and inhibiting neoplastic PD-1 (2019) Journal of Experimental and Clinical Cancer Research, 38 (1), art. no. 432, . DOI: 10.1186/s13046-019-1420-8 DOCUMENT TYPE: SOURCE: Scopus
Ieranò, C., D’Alterio, C., Giarra, S., Napolitano, M., Rea, G., Portella, L., Santagata, A., Trotta, A.M., Barbieri, A., Campani, V., Luciano, A., Arra, C., Anniciello, A.M., Botti, G., Mayol, L., De Rosa, G., Pacelli, R., Scala, S. CXCL12 loaded-dermal filler captures CXCR4 expressing melanoma circulating tumor cells (2019) Cell Death and Disease, 10 (8), art. no. 562, . DOI: 10.1038/s41419-019-1796-6
Tutte le pubblicazioni del Lab
5. CLINICAL TRIALS
Promtore dei seguenti Studi Clinici/Clinical Trials as Promoter-PI
- NKS-Ruolo delle cellule natural killer nei tumori solidi. Protocollo CEI n. 36/22 oss. (Deliberazione n.1177 del 02/12/2022).
- TRAP4MET-1 Isolamento e caratterizzazione molecolare di cellule tumorali circolanti (CTC) mediante Idrogel Belotero™ caricato con CXCL12 (CLG) in pazienti con neoplasia ovarica e polmonare in fase avanzata. Protocollo CEI n. 63/22. (Deliberazione n.267 del 26/03/2023).
- R4-FOUR-PET– Single microdose trial- CXCR4 PET tracer– Farmacocinetica e farmacodinamica di un radiofarmaco [68Ga]Ga-R54 diretto verso CXCR4 in pazienti affetti da neoplasia solida in stadio avanzato (EU CT number: 2024-513303-14-00).
- RCC-TME-Biomarcatori prognostici in pazienti affetti da neoplasia renale primitiva. Protocollo CEI n. 15/25 oss. (Deliberazione n.5397 del 25/03/2025).
Collaborazione in ambiti intra-inter dipartimentali come partecipante/Participation in other clinical trials
CIFRA: Cetuximab, Irinotecan and Fluorouracile in First-line treatment of immunologically-selected advanced colorectal cancer patients: the CIFRA study protocol in collaborazione con il Dipartimento di Oncologia Addominale. Delibera N.434 del 06/05/2019, Team member.
Arbitration: Immunological reactivity in mCRC Ras mutated treated in second line with Bevacizumab after PD with Fluo/OXA/BEVA in collaborazione con il Dipartimento di Oncologia Addominale. Delibera N.350 del 09/04/2020; Team member.
MITO35A Studio multicentrico, prospettico, a singolo braccio, di Olaparib come terapia di mantenimento in pazienti BRCA wild type con nuova diagnosi di carcinoma avanzato ovarico, delle tube di Falloppio e primitivo del peritoneo” – (Studio multicentrico no profit Delibera n. 1489 del 23/11/2021) in collaborazione con la S. C. Oncologia Clinica Sperimentale Uro-Ginecologica
MITO35B Trattamento con Olaparib oltre la progressione confrontato con chemioterapia a base di platino dopo citoriduzione secondaria in pazienti con recidiva da carcinoma ovarico. Studio di Fase III randomizzato” – (Studio multicentrico no profit Delibera n. 1489 del 23/11/2021) in collaborazione con la S. C. Oncologia Clinica Sperimentale Uro-Ginecologica
PNRR-TR1-2023-12377199 New preclinical and clinical approaches to mesothelioma, an archetypal inflammatory tumor. Studio multicentrico osservazionale no-profit (Determina Dirigenziale N. 1384 del 30/10/2024; Protocollo CEI n. 57/24 OSS) in collaborazione con IRCCS Ospedale San Raffaele di Milano.
Fornarini2023_NMIBC – PNC-E3-2022-23683266 Valutazione del ruolo prognostico/predittivo di recidiva della frequenza intratumorale di linfociti CD8+ Treg e dell’urobioma nel carcinoma della vescica non muscolo-invasivo – INNOVA – Work Package 3 (WP3- WET Lab Diagnostics). Studio multicentrico osservazionale prospettico no-profit (Determina Dirigenziale 397 del 25/03/2025; Protocollo CEI n 1/25 OSS) in collaborazione con IRCCS Ospedale Poloclinico San Martino di Genova.
PNRR-MAD-2022-12376756: Single cell dissection of the tumor microenvironment in bladder cancer for the identification of predictive tools and new therapies. (Determina Dirigenziale N.787 del 05/07/2023; Protocollo CEI n. 15-23 oss) in collaborazione con IRCCS HUMANITAS.
6. Ubicazione/Location
Quarto Piano Edificio Day Hospital/Fourth floor Day Hospital Building
